首个国产新冠特效药获批
12月8日,国家药品监督管理局应急批准腾盛华创医药技术(北京)有限公司新冠病毒中和抗体联合治疗药物安巴韦单抗注射液(BRII-196)及罗米司韦单抗注射液(BRII-198)注册申请。
这是我国首家获批的自主知识产权新冠病毒中和抗体联合治疗药物。
这两个药品可联合用于治疗轻型和普通型且伴有进展为重型(包括住院或死亡)高风险因素的成人和青少年(12—17岁,体重≥40kg)新型冠状病毒感染患者。其中,青少年适应症人群为附条件批准。
背后公司什么来头?
天眼查资料显示,腾盛华创医药技术(北京)有限公司(简称“腾盛华创”)成立于2020年5月份,注册资本约为5000万元,法定代表人为罗永庆,经营范围包括技术开发、技术咨询、技术转让、药品委托生产、药品零售等。
从股权结构来看,腾盛华创的控股股东是腾盛博药医药技术(香港)有限公司,系香港上市公司腾盛博药-B(02137.HK)的全资孙公司。第二大股东是由深圳卫健委、深圳市第三人民医院举办的深圳国家感染性疾病临床医学研究中心,持股13.34%。
据悉,此次获批的新冠抗体药物由清华大学、深圳市第三人民医院和腾盛博药合作研发。今年10月,腾盛博药向药监局提交了上述两种特效药的紧急使用授权申请。
中和抗体疗法,简单地说就是人为地补给抗体来支援免疫系统。有研究报告预计,中和抗体整体市场体量将达到80亿-100亿美元。
三天前,腾盛博药-B刚公告称,在研的新型冠状病毒联合疗法(即安巴韦单抗/罗米司韦单抗联合疗法),在疾病进展高风险的门诊患者中,住院及死亡的复合终点降低80%,治疗组受试者在28天治疗期内无死亡,而安慰剂组有9例死亡。
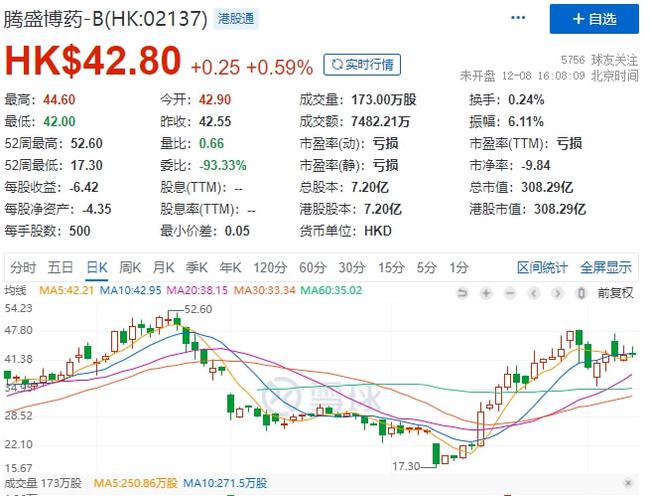
屡屡公布药物研发顺利进展,腾盛博药-B近20个交易日以来已累计涨逾120%。
据统计,全球已有20款中和抗体药物获批临床,国内在研治疗新冠中和抗体药物不低于10款,近期也有不少企业公布临床实验情况。
这些公司新冠药物也在研发中
除腾盛博药的上述两款特效药外,国内君实生物的新冠药物研发进展也不慢。
12月5日,君实生物表示,在预防和治疗COVID-19上,已领先布局了2项中和抗体及1项小分子口服药物。
其中,抗体类新药JS026注射液的临床试验申请已于11月份获得国家药监局批准。目前,公司正在积极评估该抗体对于最新突变株奥密克戎的中和作用。
埃特司韦单抗(JS016/LY-CoV016)的安全性及有效性已获得世界性认可。目前,埃特司韦单抗1400mg和巴尼韦单抗(LY-CoV555)700mg双抗体疗法已在全球15个国家或地区获得紧急使用授权。
之江生物、绿叶制药、迈威生物、国药集团等药企的新冠中和抗体药物研发工作也在有序推进中。
编辑:齐少恒
相关热词搜索: 首个国产新冠特效药获批







